感染症医のための非劣性試験の読み方(3/3)
新薬が標準薬に非劣性を示したら標準薬に取って代わることができるか?
ある疾患の標準治療薬に対して新しい治療薬の非劣性が証明された場合、この新しい治療薬は標準薬に取って代わるだろうか。治療効果が劣らないうえに、従来の標準治療薬よりも副作用が少ない、コストが安い、投与がしやすいなどの条件を満たせば取って代わることはあり得るだろう。しかし、非劣性試験はその試験デザインの性質上、「臨床的に問題になるほど劣らない非劣性マージン」の範囲で劣る可能性を許容する。
例えば、ある疾患に対する標準治療薬Aのプラセボに対する効果が80%高いとした場合を考える。Aに対して治療効果が10%劣ることを許容して治療薬Bが非劣性を示し、Bが標準治療薬に取って代わったとする。次に、Bを基準薬として治療薬Cが10%の非劣性マージンで非劣性が証明されたとする。これを10回繰り返すと、10回目の治療薬Kは理論的には治療薬Aに非劣性ということになるが、実際の治療効果はプラセボに対して28%まで目減りしてしまう可能性をはらむ。この現象は“bio-creep”と呼ばれる。
Everson-Stewartらのシミュレーションによれば、constancy assumption(基準薬の過去のプラセボ比較試験と非劣性試験の類似性)が保たれている限りはbio-creep現象の出現はまれであったが、constancy assumptionに違反があればbio-creepが高率に出現すると試算されている[1]。CONSORT(Consolidated Standards of Reporting Trials)声明拡張版でも、基準薬が有効性を示した過去のプラセボ比較試験と参加者や介入、治療評価尺度が類似していることを要求しているが、具体的にどの程度類似しているかを検証する方法は明記されていない。
感染症領域では非劣性試験が実施されることが多くなっていることは既に述べた[2]。ガイドラインの推奨根拠として非劣性試験の結果が引用されることも少なくないが、非劣性試験のエビデンスレベルをランダム化比較試験(randomized controlled trial;RCT)だからといって優越性試験のRCTと同列に扱ってよいかは疑問に思う。
例えば、黄色ブドウ球菌菌血症に対してダプトマイシンは標準治療薬(MRSAの場合はバンコマイシン、MSSAの場合は抗ブドウ球菌用ペニシリン)に非劣性を示したRCTが1つ存在するのみであるが[3]、米国感染症学会(Infectious Diseases Society of America;IDSA)および国内のMRSA感染症ガイドラインにおいてダプトマイシン(A-I)のほうがバンコマイシン(A-II)よりもエビデンスレベルが高く設定されている[4、5]。これはRCTが1件でもあればエビデンスレベルがIになり、RCTがなければエビデンスレベルがIIと分類されるためである。しかし、バンコマイシンにRCTがないのは、長年の間、MRSAの血流感染症に対して標準治療薬とされてきて、プラセボとの比較試験が倫理的に困難だったからである。標準治療薬に1回だけ非劣性を示したダプトマイシンのほうがエビデンスレベルが高くなるのは、論理的に納得しがたい。
一般にRCTのエビデンスレベルは観察研究のそれよりも高いとされるが、これは単に研究デザインの質を評価しているだけで、RCTであれば自動的に質が高いという意味ではない。バイアスの多いRCTのほうがバイアスの少ない観察研究よりも本当に質が高いかどうかは一考する必要がある。
診療ガイドラインが「研究デザインに分類されたエビデンスの質」にのみ依存していたり、様々なガイドラインが独自のエビデンス評価システムを作成していたりする現状に対して、エビデンスの質と推奨を分離し、世界中の多くのグレーディングを統一しようというのがGRADEシステムである。GRADEシステムでは、RCTでもバイアスや限界が多ければエビデンスの質が低くなることがあり、観察研究でもバイアスが少なかったり効果量が高かったりすれば質が高く評価される。GRADEシステムについての詳細は別途ウェブサイトを参照してほしい[6]。
感染症領域の臨床試験の今後
新しい感染症治療薬の有効性を検証する際、従来の優越性試験のみでは困難である。優越性試験と非劣性試験の利点と欠点を理解したうえで双方を組み込む研究デザインについてIDSAがwhite paperを出版しており、そこで提唱されている研究デザインを紹介する[7]。
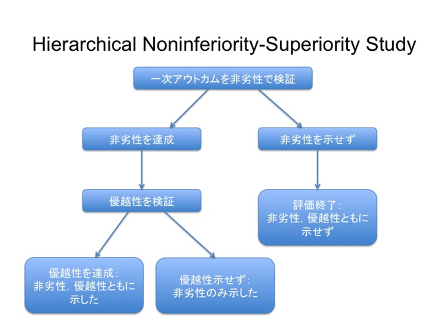
図1はHierarchical Noninferiority-Superiority Studyと呼ばれ、プライマリーアウトカムは非劣性で検証し、非劣性を示したら優越性の検証を行う[7]。 適切な非劣性マージンを設定し、検出力を設定しておく必要がある。 MRSAによる病院内肺炎治療のリネゾリドとバンコマイシンの比較試験で用いられた[8]。
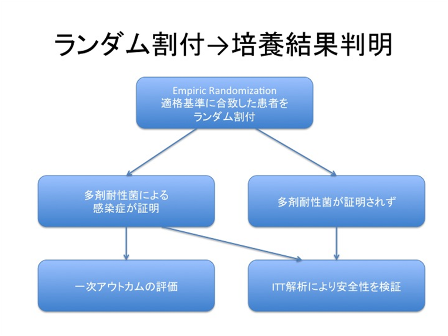
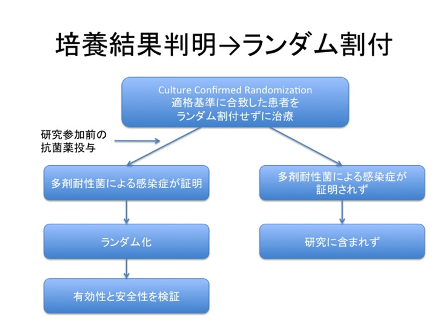
多剤耐性菌を標的にした治療薬の有効性を評価する際には、どの時点で患者をランダム割付するかが問題になる。図2では、培養結果が判明する前に患者のランダム割付を行っている。耐性菌が検出された症例に対してのみ一次アウトカムを検証するため、ランダム化は崩れてしまう。 耐性菌が検出されなかった症例も含めて、intention-to-treat (ITT)解析で安全性を検証する[7]。図3は、培養結果が判明してからランダム割付を行っている。こちらのほうが診断と起因菌が確定した患者のみにランダム割付を行うので分かりやすいかもしれないが、多くの場合、培養結果が判明するまで治療を待つことができないため、研究開始前に抗菌薬が開始されている影響が出てしまうという欠点がある[7]。
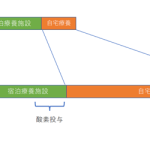
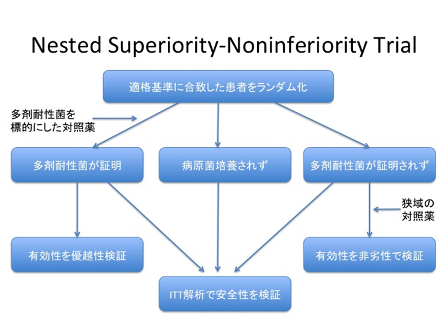
より複雑なものとして図4のようなものがある。これは、耐性菌が検出された症例のみ有効性について優越性を検証し、 耐性菌が検出されなかった症例では狭域の対照薬と有効性の非劣性試験を行い、 すべての症例を対照にITT解析で安全性検証を行うものである[7]。
おわりに
これまで述べてきたことを踏まえて、黄色ブドウ球菌菌血症に対するダプトマイシンと標準治療を比較した非劣性RCTの結果を眺めてみよう[3]。
一次アウトカムは治療終了後42日後のclinical successになっている。臨床的治療失敗、微生物学的治療失敗、死亡、血液培養採取せず、試験薬以外に有効な抗菌薬の投与、臨床的失敗や微生物学的失敗、副作用による試験薬の早期中止が評価時のfailureと定義されているので、これらがない場合にclinical successと判断したようである。死亡以外のイベントに関しては評価者の主観が入りうるが、どのように評価者の客観性を担保したのかが論文上は不明確である。
また、一次アウトカムについて非劣性マージンを20%に設定しているが、この設定の根拠もはっきりしない。各アウトカムに対する治療効果の信頼区間を図示したFigure1を眺めると(著作権の関係で図を示せないため、各自ご確認いただきたい)、非劣性マージンをいくらに設定するかによって統計学的な結論は変わってしまいそうに見える。
ダプトマイシンを販売している会社が資金を提供した研究であり、評価者によりダプトマイシンに有利な判断がなされた可能性を差し引く必要があるが、少なくともどちらかの群が極端に悪いということはなさそうなので、臨床的な解釈として大きな差はなさそうというのが筆者の解釈である。やはり、この結果だけを見て、黄色ブドウ球菌菌血症の治療にダプトマイシンを優先する気にはならない。
「RCTで非劣性を示した」という文言を見たときに「劣っていないとはどういうことか?」を考える一助に本稿がなれば幸いである。
【References】
1)Everson-Stewart S,Emerson SS:Bio-creep in non-inferiority clinical trials.Stat Med.2010 Nov 30;29(27):2769-80.
2)Lange S,Freitag G.Choice of delta:requirements and reality―results of a systematic review.Biom J.2005 Feb;47(1):12-27;discussion 99-107.
3)Fowler VG Jr,Boucher HW,Corey GR,et al:Daptomycin versus standard therapy for bacteremia and endocarditis caused by Staphylococcus aureus.N Engl J Med.2006 Aug 17;355(7):653-65.
4)Liu C,Bayer A,Cosgrove SE,et al:Clinical practice guidelines by the infectious diseases society of america for the treatment of methicillin-resistant Staphylococcus aureus infections in adults and children.Clin Infect Dis.2011 Feb 1;52(3):e18-55.
5)MRSA感染症の治療ガイドライン作成委員会:MRSA感染症の治療ガイドライン,2013.
6)相原守夫:GRADEシステムと診療ガイドライン作成とEBMとシステマティックレビュー.http://www.grade-jpn.com
7)Infectious Diseases Society of America:White paper:recommendations on the conduct of superiority and organism-specific clinical trials of antibacterial agents for the treatment of infections caused by drug-resistant bacterial pathogens.Clin Infect Dis.2012 Oct;55(8):1031-46.
8)Wunderink RG,Niederman MS,Kollef MH,et al:Linezolid in methicillin-resistant Staphylococcus aureus nosocomial pneumonia:a randomized,controlled study.Clin Infect Dis.2012 Mar 1;54(5):621-9.
(了)